Damos la bienvenida a la primera licencia abierta de una prueba de COVID-19 para el fondo de acceso tecnológico de la OMS
El Consejo Superior de Investigaciones Científicas firma un acuerdo de licencia de acceso abierto de sus test serológicos.
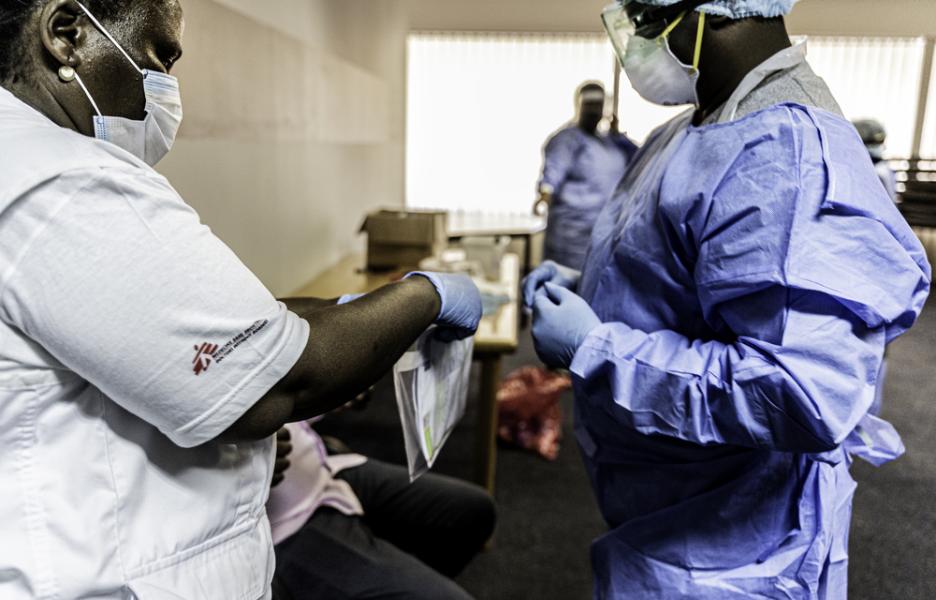
Acogemos con satisfacción el anuncio del fondo de acceso a tecnología COVID-19 de la OMS (conocido por sus siglas en inglés C-TAP) y el Medicines Patent Pool (MPP) de la primera licencia voluntaria global, no exclusiva y transparente para una prueba de diagnóstico COVID-19.
La tecnología, ofrecida por el Consejo Superior de Investigaciones Científicas (CSIC), es una prueba de anticuerpos capaz de cuantificar tres tipos diferentes de anticuerpos, y diferenciar las personas vacunadas de las que se han infectado de forma natural por COVID-19, con fines de vigilancia de salud pública. Con la puesta en marcha de los programas de vacunación, esta prueba es muy importante para medir el número de casos de COVID-19 en un país y el impacto de las medidas de control.
Desde diciembre de 2020, la OMS recomienda el uso de inmunoensayos cuantitativos (ELISA) para la vigilancia de COVID-19. Contar con pruebas fiables para la vigilancia de COVID-19 es fundamental para medir la incidencia y la mortalidad, y qué grupos de población tienen mayor riesgo. Hasta hoy, la OMS solo tenía una prueba ELISA de anticuerpos precalificada en su lista de uso de emergencia, la prueba ELISA Elecsys Anti-SARS-CoV-2 de Roche, una gran corporación farmacéutica con sede en Suiza. Esta prueba solo se puede utilizar con el propio dispositivo de Roche, que no está disponible ni es adecuado para la mayoría de entornos con recursos limitados. Muchas pruebas ELISA disponibles en el mercado solo pueden identificar uno o dos tipos de anticuerpos.
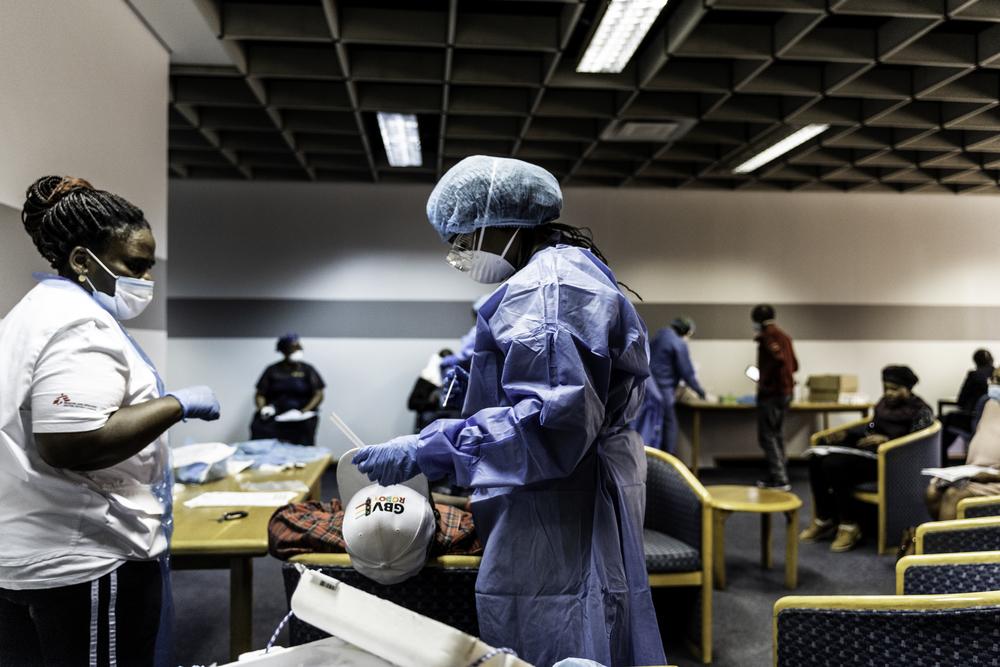
La licencia abierta del CSIC al fondo C-TAP de la OMS es un importante paso adelante para superar el monopolio de las grandes empresas de diagnóstico como Roche, y para facilitar la producción y el suministro de pruebas de anticuerpos ELISA fiables en todos los países.
Sin embargo, solo una licencia de un propietario de tecnología no es suficiente para que los desarrolladores de determinados países puedan mejorar sus pruebas de anticuerpos COVID-19 y facilitar el acceso. Eliminar las barreras de propiedad intelectual en todos los componentes tecnológicos claves y facilitar un intercambio abierto, puesta en común y transferencia de tecnologías, datos y conocimientos es importante para garantizar y mejorar el acceso a los diagnósticos de COVID-19 para todos.
Declaraciones de Stijn Deborggraeve, asesor de Diagnóstico de nuestra Campaña de Acceso a Medicamentos Esenciales:
“MSF acoge con satisfacción el anuncio de la primera licencia abierta voluntaria y transparente para una prueba de diagnóstico de COVID-19. Dado que la OMS recomienda la prueba de anticuerpos ELISA para la vigilancia de COVID-19, esperamos que la licencia abierta de esta tecnología acelere ahora la producción local de esta prueba en países de ingresos bajos y medios para respaldar la vigilancia de COVID-19.
La falta de acceso a pruebas de diagnóstico fiables es un desafío en muchos países de ingresos bajos y medios, en parte debido al acceso limitado a tecnologías patentadas por parte de los fabricantes de diagnóstico locales, lo que hace que estos países dependan en gran medida de las pruebas de diagnóstico importadas de Estados Unidos, Europa y Asia. Durante la pandemia, hemos sido testigos del acaparamiento no solo de vacunas y tratamientos, sino también de pruebas de diagnósticos de COVID-19, lo que ha dejado a muchos países de ingresos bajos y medios sin los muy necesarios test para ayudar a controlar la COVID-19.
En esta pandemia, el acceso a pruebas de diagnóstico fiables es el primer y más importante paso para salvar vidas, y medir los casos de COVID-19 y el impacto de las intervenciones. No es lógico que incluso en olas catastróficas de esta enfermedad, que han provocado millones de muertes en todo el mundo, las corporaciones de diagnóstico hayan continuado monopolizando y acumulando pruebas críticas de COVID-19 para un puñado de personas y países privilegiados.
Aunque la OMS ha recomendado el uso de inmunoensayos basados en ELISA para la vigilancia en salud pública de COVID-19 desde diciembre de 2020, Roche sigue siendo el único proveedor aprobado por la OMS. Y Roche sigue negándose a compartir abiertamente esta tecnología con otros fabricantes. La licencia al fondo C-TAP de la OMS es un paso prometedor para romper monopolios como el de Roche y permitir que todos los países desarrollen y fabriquen esta tecnología que salva vidas.
Pero dado que las grandes corporaciones continúan teniendo monopolios sobre la mayoría de las tecnologías de salud COVID-19, esta exitosa licencia de una prueba de diagnóstico para el fondo C-Tap de la OMS debe complementarse con la adopción de la propuesta de exención de los ADPIC en el reunión ministerial de la Organización Mundial del Comercio la próxima semana que tiene como objetivo suspender la propiedad intelectual de todas las herramientas médicas de COVID-19, incluidos los diagnósticos”.
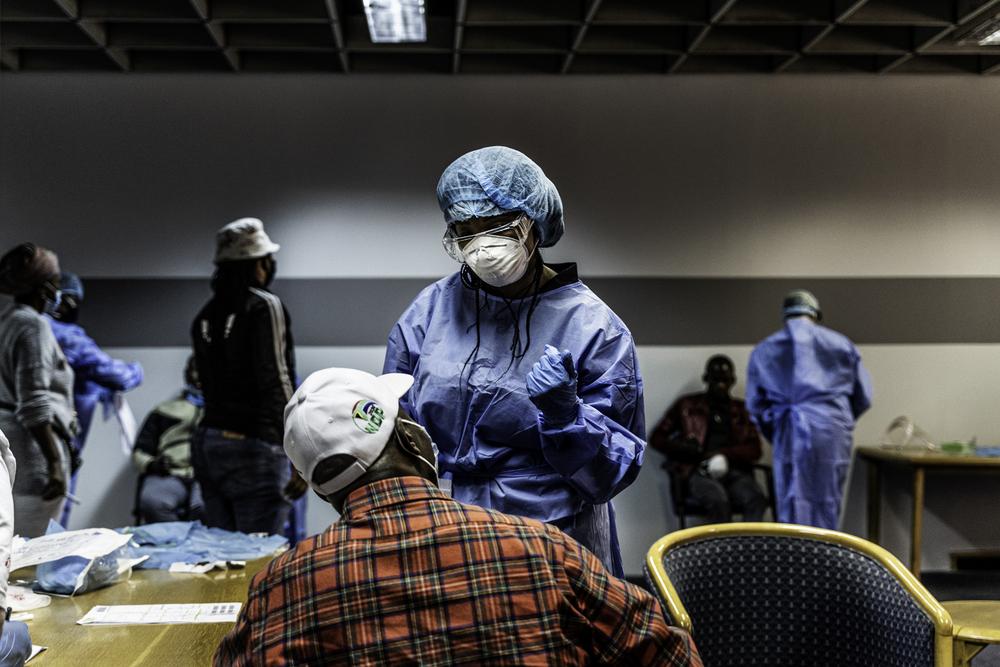
Declaraciones de Raquel González, nuestras responsable de Relaciones Institucionales:
“El acuerdo firmado entre el CSIC, la OMS y el MPP representa la primera licencia abierta, transparente, global y no exclusiva para una herramienta de COVID-19 desde que empezó la pandemia y esperamos que facilite la fabricación y comercialización de la prueba serológica COVID-19 del CSIC en todo el mundo, especialmente en países de ingresos bajos y medios, ayudando así al control de la pandemia.
La cesión de la licencia abierta de su test serológico para COVID-19 muestra la decidida apuesta del CSIC y el Gobierno por una ciencia al servicio de la salud pública, que quiere contribuir a la respuesta global que exige una pandemia. El acuerdo también es un paso adelante muy importante en modelos de colaboración que permiten compartir el conocimiento y la tecnología en aras del bien común y a un precio justo.
Paralelamente a acuerdos tan importantes como el anunciado entre el CSIC, la OMS y el MPP hay que impulsar otras iniciativas, como la exención de la propiedad intelectual para herramientas COVID-19, que lleva más de un año discutiéndose en la Organización Mundial del Comercio, y que ayudarían también a extender la rápida fabricación y distribución de pruebas de diagnóstico, tratamientos y vacunas contra COVID-19 que se requiere dada la urgencia de la situación actual”.